Configuración electrónica del Rutherfordio
 La configuración electrónica del rutherfordio es 5f 14 6d 2 7s 2. Este es un elemento químico que anteriormente recibía el nombre de Kurchatovio; En nuestra tabla periódica se encuentra simbolizado como Rf y su número atómico es 104.
La configuración electrónica del rutherfordio es 5f 14 6d 2 7s 2. Este es un elemento químico que anteriormente recibía el nombre de Kurchatovio; En nuestra tabla periódica se encuentra simbolizado como Rf y su número atómico es 104.
Recibe el nombre de rutherfordio en honor al físico británico y científico que colaboró al modelo atómico y la física nuclear Ernest Rutherford.
Configuración electrónica del Rutherfordio
Sus electrones por capa son: 2, 8, 18, 32, 32, 10, 2 como se presenta a continuación: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 4f14 5d10 6s2 6p6 5f14 6d2 7s2
Descubrimiento del Rutherfordio
El año 1964 fue la vez primera que se sintetizó el rutherfordio en el Instituto Conjunto de Investigación Nuclear en Dubná. Para sintetizar los investigadores bombardearon una diana de plutonio-242 con iones de neón -22.
En 1969 se sintetizó de forma definitiva por los investigadores de la Universidad de California en Berkeley en la que bombardearon californio -249 con iones de carbono-12.
Isótopos del Rutherfordio
Como el Rutherfordio no es un elemento dado de manera natural sino que es producido sus isótopos tampoco lo son.
Hasta el momento se han sintetizado varios isótopos radiactivos dentro de laboratorios, informando la existencia de 16 isótopos diferentes con masas atómicas entre 253 y 270, ya sea el origen de estos mediante la fusión de dos átomos o por medio de la desintegración de elementos más pesados; las masa atómicas son variables en el caso del isótopo 264 y el 270. La mayoría de los isótopos del rutherfordio se descomponen por vías de fusión espontánea.
Los isótopos del rutherfordio son:
- 253 Rf, descubierto en el 1994.
- 254 Rf, descubierto en el 1994.
- 255 Rf, descubierto en 1974.
- 256 Rf, descubierto en 1974.
- 1957 Rf, descubierto en 1969.
- Los 257m Rf, descubierto en 1969, al conjunto de:
- 258 Rf
- 259 Rf
- 259m Rf
- 260 Rf
- 261 Rf descubierto en 1970.
- 261m Rf, descubierto en 2001.
- 262 Rf, descubierto en 1996.
- 263 Rf, descubierto en 1999.
- 263m Rf, descubierto en 1999.
- 265 Rf, descubierto en 2010.
- 266 Rf
- 267 Rf, descubierto en el 2004.
- 268 Rf
- 270 Rf.
Tiempo de vida de los isótopos del Rutherfordio
De los isótopos que hasta hora sus vidas medias se han conocido, los isótopos más ligeros resultan ser los más inclinados a un tipo de vida medias cortas.
Se han observado isótopos que presentar una semivida de menos de μs como es el caso del 253 Rf y el 254Rf. Aunque por otro lado, también encontramos los isótopos 258 Rf y el 260 Rf que presentan una vida más estable de alrededor a los 10 minutos.
Por lo general, los isótopos más pesados resultan siendo los más estables, encontrando en este renglón al isótopo 267 Rf con una vida media de 1,3 horas aproximadamente.
Características físicas y atómicas del Rutherfordio
- Se desconoce el estado original del rutherfordio bajo condiciones normales, sin embargo se espera que sea un sólido.
- Se presume es un metal común una densidad de alrededor 23,2g/cm3 por lo que se cree es muy pesado.
- Pertenece al grupo de los metales en transición.
- Pertenece a la familia del titanio.
- Es un metal, radiactivo y sintético.
- En su fase gaseosa, al presentar enlaces más covalentes, el cloruro de rutherfordio es más volátil que el cloruro de hafnio, que se supone es su homólogo más ligero.
- Tiene una masa atómica de 261u.
Características químicas del Rutherfordio
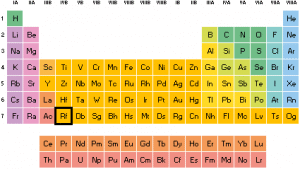 Es el segundo miembro de un total de 66 metales de transición y el primer elemento transactínido.
Es el segundo miembro de un total de 66 metales de transición y el primer elemento transactínido.- Sus propiedades son semejantes a las presentadas en el grupo 4.
- En nuestra tabla periódica, lo encontramos con la simbología Rf, ubicada en el número 104 de nuestra tabla periódica correspondiente a su número atómico.
- Corresponde al periodo 7, bloque d y grupo 4.
- Al calcular su radio atómico, energías orbitales, potenciales de ionización y sus niveles terrestres se llegó a la conclusión que los estados que este elemento presentaba respecto su ionización son muy similares a las del hafnio.
Aplicaciones del Rutherfordio
El rutherfordio es un elemento muy inestable, recordemos que es un transfermio y su uso es solo para la realización de estudios científicos, al menos hasta hoy día.
Daños del Rutherfordio a la salud y el medio ambiente
Como es un elemento inestable y la cantidad que se utiliza cada formación de este se descompone,hasta el momento no se han estudiado los daños que este puede provocar a la salud humana y el medio ambiente, sin embargo se recomienda tener precaución a la hora de manipular este elemento.


También te puede interesar...